近日,食品与生物工程学院李玲、何宇新教授团队在《Food Research International》发表题为“Natural polyphenols in the treatment of IBD: pathological intervention activities and delivery system constructions”的综述性论文。食品与生物工程学院研究生张宜为论文第一作者,李玲教授及何宇新教授同为本文通讯作者。

论文摘要
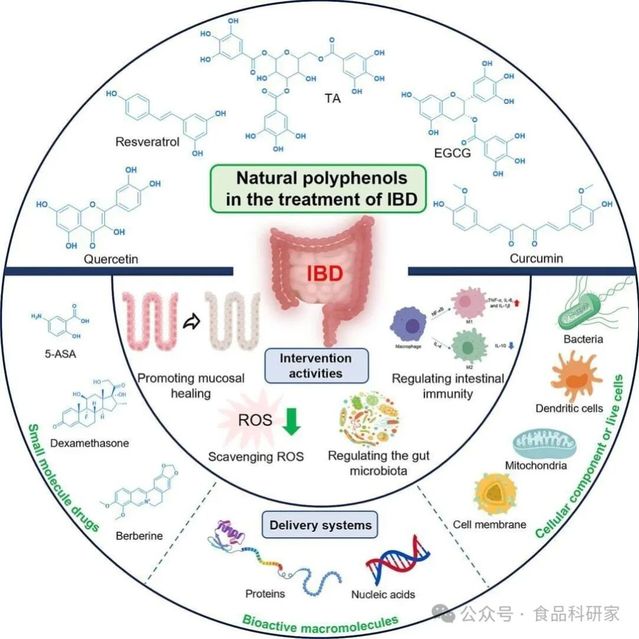
炎症性肠病(IBD)的发病机制涉及遗传、环境、肠道菌群失调与免疫紊乱的相互作用,目前高效治疗策略仍较为有限。天然多酚是一类源自植物的生物活性化合物,凭借其强大的抗炎、抗氧化及免疫调节特性,在IBD治疗中展现出巨大潜力。本综述从四个核心机制总结了多酚在IBD治疗中的作用,包括促进黏膜愈合、实现抗氧化与铁螯合、调节肠道菌群及调控肠道免疫。此外,我们系统综述了各类基于多酚的治疗性药物递送系统在 IBD 治疗中的显著潜力,涵盖人工小分子药物、天然来源化合物、生物活性蛋白、核酸类治疗剂以及细胞成分与活细胞等多种递送对象。同时,结合临床应用需求,探讨了该领域面临的局限性与未来展望。本综述聚焦多酚的药学特性及 IBD 治疗中递送系统的功能设计,为开发创新性治疗方案提供理论依据。
研究背景
炎症性肠病(IBD)是一类以肠道慢性炎症为主要特征的胃肠道疾病,主要包括克罗恩病(CD)和溃疡性结肠炎(UC),其发病与肠道屏障损伤、肠道菌群失衡、免疫过度激活及环境因素密切相关,患者常表现为持续腹泻、腹痛、组织损伤等症状,严重影响生活质量。全球 IBD 发病率持续上升,预计 2030 年中国患者人数将接近 120 万,已成为重要的公共卫生挑战。目前临床常用治疗药物如5-氨基水杨酸、糖皮质激素、免疫抑制剂等,长期使用易引发肝毒性、免疫功能受损、耐药性等问题,亟需开发安全高效的新型治疗策略。天然多酚广泛存在于植物中,具有结构多样性和多靶点药理活性,不仅能通过清除活性氧、修复肠道屏障、调节菌群平衡及免疫稳态发挥抗炎作用,其分子结构中的酚羟基还可通过氢键、疏水作用等与生物分子相互作用,兼具治疗剂与递送系统功能材料的双重潜力。然而,多酚自身存在生物利用度低、化学稳定性差、易被氧化降解等局限,限制了其临床应用。基于此,深入解析多酚干预 IBD 的分子机制,构建高效靶向递送系统以提升其生物利用度与治疗效果,已成为 IBD 治疗领域的研究热点,对推动天然多酚类疗法的临床转化具有重要意义。
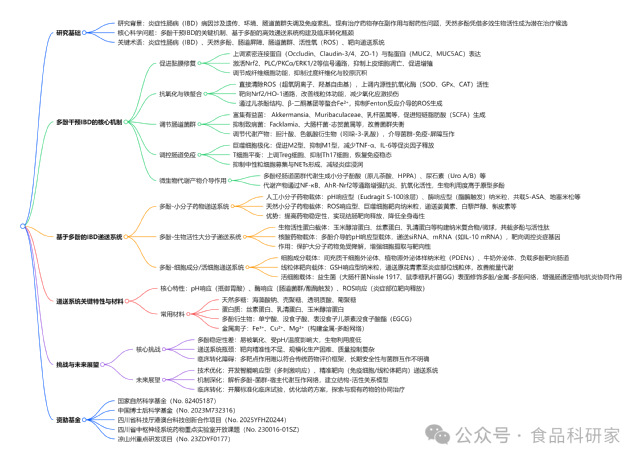
图文欣赏
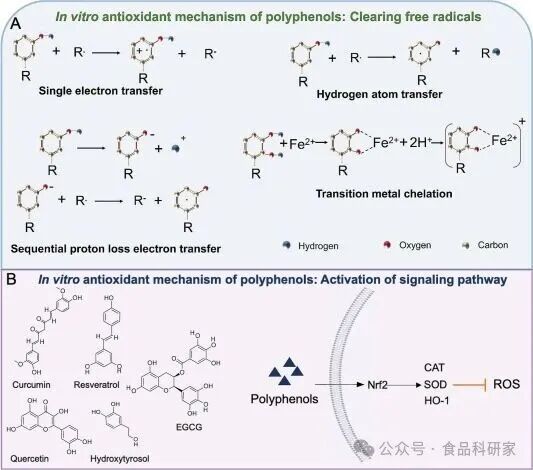
Figure 1 多酚的抗氧化机制(图示多酚体外抗氧化原理:清除自由基的化学过程)
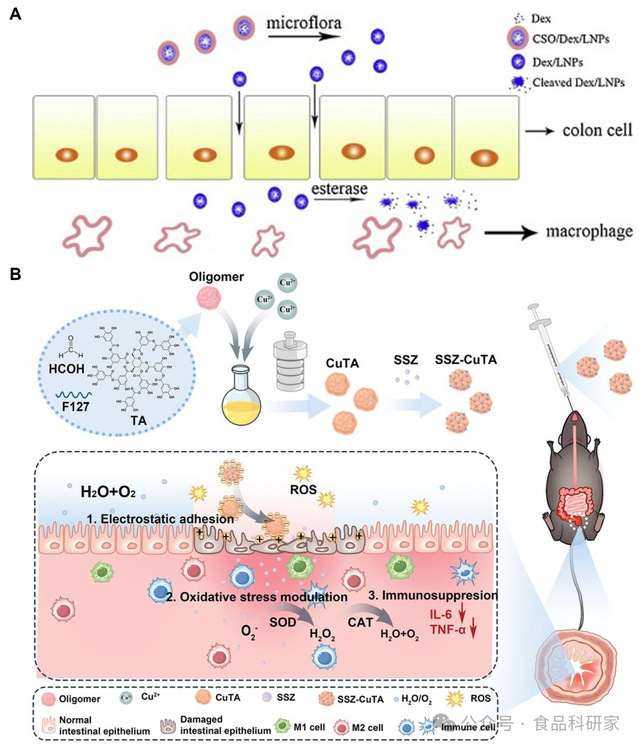
Figure 2 用于IBD治疗的多酚 - 人工小分子药物递送系统
(A)Qu-SS-Gcc LNPs 纳米平台用于溃疡性结肠炎(UC)的靶向响应性药物递送机制示意图(Chen et al., 2020);(B)SSZ-CuTA 的合成及其体内治疗 IBD 的作用示意图(Yan et al., 2024)
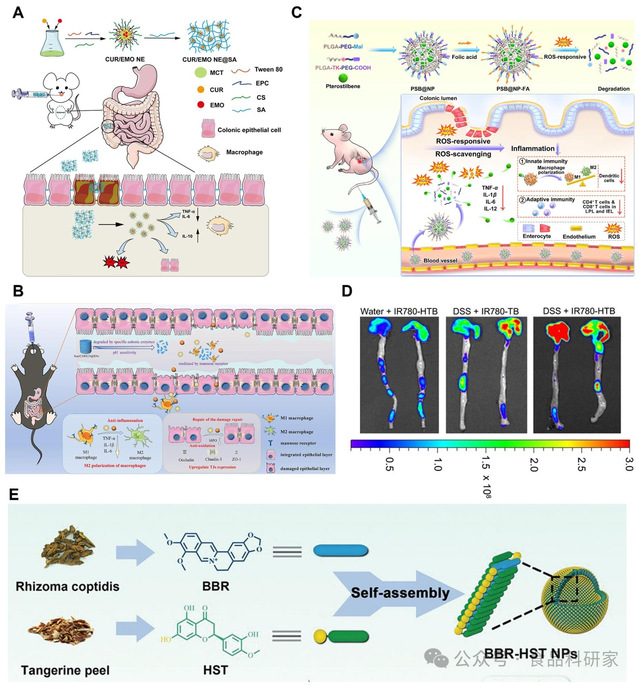
Figure 3 用于 IBD 治疗的多酚 - 天然小分子药物递送系统
(A)通过高能乳化法制备姜黄素 / 大黄素纳米乳(CUR/EMO NE),并经物理交联构建海藻酸钠(Alg)水凝胶包覆制剂(CUR/EMO NE@SA)的示意图,及其通过协同抗炎和促进肠黏膜修复治疗 IBD 的作用机制(Lei et al., 2023);(B)Kae/CMCHD@RNs 的结肠靶向特性及体内抗 UC 治疗示意图(Tang et al., 2025);(C)活性氧(ROS)响应型纳米载体改善小鼠结肠炎的示意图(Yan, Regenstein, et al., 2023);(D)TB 和 HTB 在体内的黏附效果(Chen, Hao, et al., 2022);(E)小檗碱(BBR)与橙皮素(HST)通过自组装形成无载体、多功能球形纳米颗粒(BBR-HST NPs)的示意图(Gao et al., 2023)
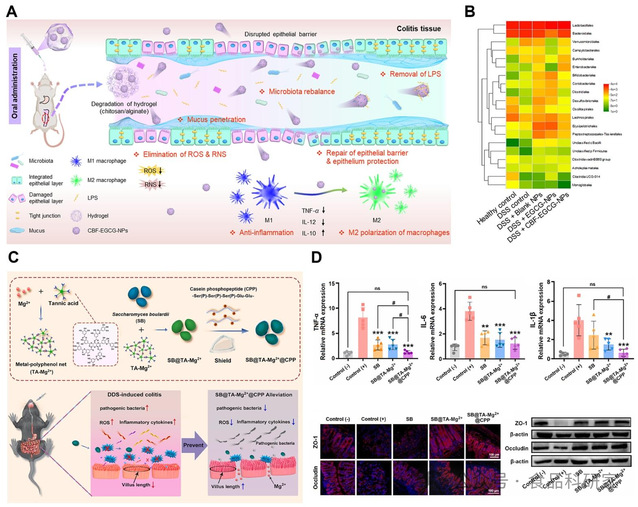
Figure 4 用于 IBD 治疗的多酚 - 生物活性蛋白递送系统
(A)口服抗菌肽 - EGCG 纳米药物协同治疗 UC 的示意图(Liu, Chen, et al., 2022);(B)CBF-EGCG-NPs 调控肠道菌群的效果(Liu, Cao, et al., 2022);(C)SB@TA-Mg²⁺@CPP 的制备及其预防 UC 的多功能机制示意图(Qian et al., 2025);(D)摄入 SB@TA-Mg²⁺@CPP 对肠道屏障改善的作用(Qian et al., 2025)
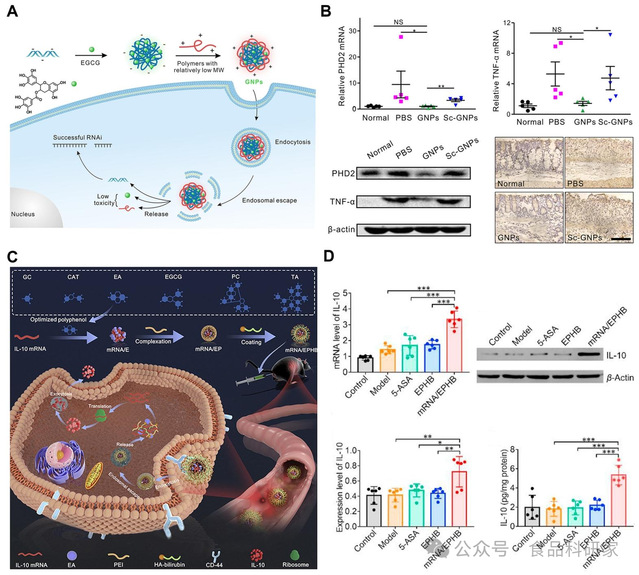
Figure 5 用于 IBD 治疗的多酚 - 核酸药物递送系统
(A)绿色纳米颗粒(GNPs)的制备及其基因沉默机制示意图(Shen et al., 2018);(B)GNPs 在 DSS 诱导的肠道损伤模型中的治疗效果(Shen et al., 2018);(C)以多酚化合物为功能成分的 IL-10 mRNA 递送平台示意图(Chen, Hao, et al.,2022);(D)该递送平台在急性 UC 模型中的疗效评估(Chen, Hao, et al., 2022)
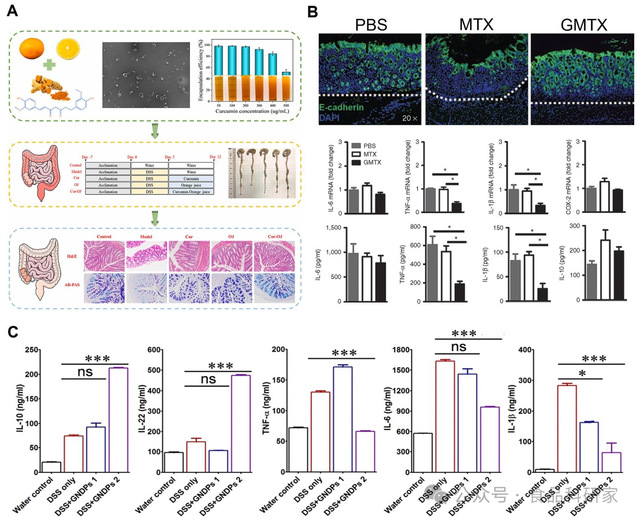
Figure 6 用于 IBD 治疗的多酚 - 细胞成分递送系统
(A)柑橘来源的细胞外囊泡作为天然生物活性纳米载体,制备具有缓解结肠炎特性的姜黄素强化橙汁的示意图(Liu et al., 2024);(B)GMTX 在急性结肠炎中的疗效(Wang, Zhou, et al., 2014)(C)采用酶联免疫吸附法测定结肠组织中炎症介质的浓度(Zhang et al., 2016)
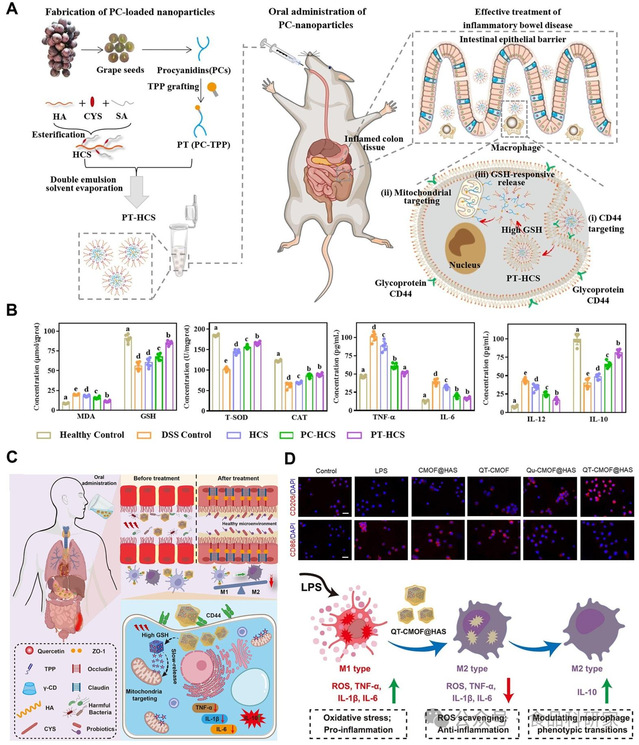
Figure 7 用于 IBD 治疗的多酚 - 细胞成分 / 活细胞介导的递送系统
(A)原花青素(PCs)口服递送系统的构建示意图:将原花青素与线粒体靶向三苯基膦(TPP)衍生物偶联,并包覆透明质酸(HA)外壳(Tie et al., 2022);(B)结肠炎小鼠结肠组织中氧化应激相关指标及炎症细胞因子的水平(Tie et al., 2022);(C)槲皮素(Qt)-CMOF@HAS 纳米立方体的调控机制示意图(Zhao, Chen, et al., 2025);(D)Qt-CMOF@HAS 纳米立方体的抗氧化应激和抗炎能力(Zhao, Chen, et al., 2025)
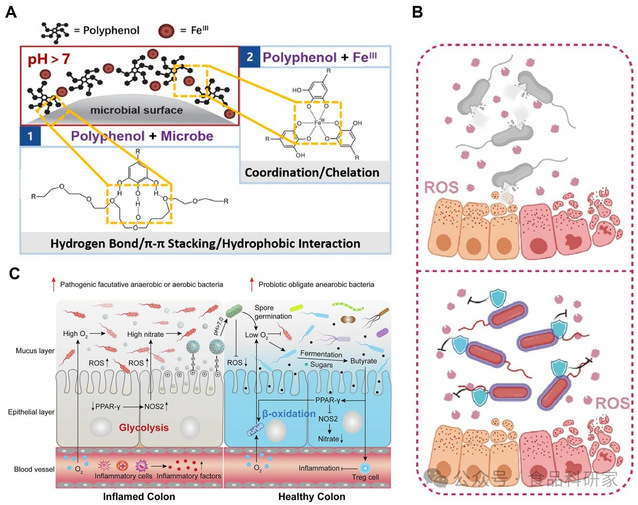
Figure 8 用于 IBD 治疗的多酚 - 活细胞介导的递送系统
(A)白藜芦醇(RSV)与 Li01 联合治疗对 DSS 诱导的结肠炎小鼠血清 5 - 羟色胺(5-HT)浓度的影响(Fei et al., 2022);(B)工程化生物制剂治疗 DSS 诱导的结肠炎的作用机制示意图(Chen, Qiao, et al., 2023);(C)“超级肠道微生物(SGM)” 靶向 ROS 的示意图(Yang et al., 2022)
研究结论
天然多酚凭借其抗氧化、抗炎及免疫调节生物活性,在炎症性肠病(IBD)治疗中展现出双重应用潜力:既可作为治疗药物缓解病理变化,也可作为构建药物递送系统的重要材料。本综述系统总结了多酚干预IBD的四大机制,并全面梳理了各类多酚介导的药物递送系统在IBD治疗中的应用进展。
尽管多酚基递送系统作为“治疗-递送一体化”策略具有天然来源、良好降解性及协同疗效等优势,但其临床转化仍面临多重挑战:化学组成复杂、标准化难度大、工艺放大困难,且长期安全性数据尚不充分。目前相关研究多局限于实验室阶段,其药代动力学特性、体内安全性及监管路径仍有待阐明。未来需深入开展机制研究、完善生物安全性评估,并探索个性化治疗适配方案,以推动多酚基系统从实验室走向临床应用,为IBD治疗提供新的解决方案。














