近日,西华大学余孝其教授团队与四川大学李坤教授团队合作在国际顶级期刊《Science Bulletin》(IF = 21.1)发表题为“Precise molecular spacer engineering for tumor-responsive pKa tuning: a pan-cancer imaging platform for evaluating tumor microenvironment reprogramming capability” 的研究论文,提出基于间隔基的分子工程创新策略,实现pH传感探针的精准pKa调控,为泛癌成像、转移灶成像及肿瘤微环境重塑监测提供技术支持。

图1 论文截图
由于肿瘤代谢异常导致的pH稳态失衡已成为实体肿瘤的共性标志,开发pKa可调的pH荧光探针是实现肿瘤精准成像的关键。然而,现有探针构建思路多依赖直接修饰荧光团,且难以满足泛癌及转移灶成像需求。为此,研究团队以meso位氨基取代的砜-呫吨荧光骨架为基础,基于暗态亚胺形式与荧光烯胺形式之间的异构化pH传感机制,通过在meso位氨基引入强吸电的三氟甲基,同时分别插入1、2、3个亚甲基间隔基,成功将探针的 pKa 值由7.07调控至3.73、5.37和5.87(图1)。理论计算揭示,三氟甲基可通过延长 N-H 键促进质子解离,且随着间隔基数量的增加,调控效率递减,因而pKa值逐渐升高。这种通过非共轭三氟甲基实现的“远程”调控策略,区别于现有直接作用于荧光团的“近程”调控方式(如受体工程、给体工程和杂原子工程),被作者命名为“间隔基分子工程”。
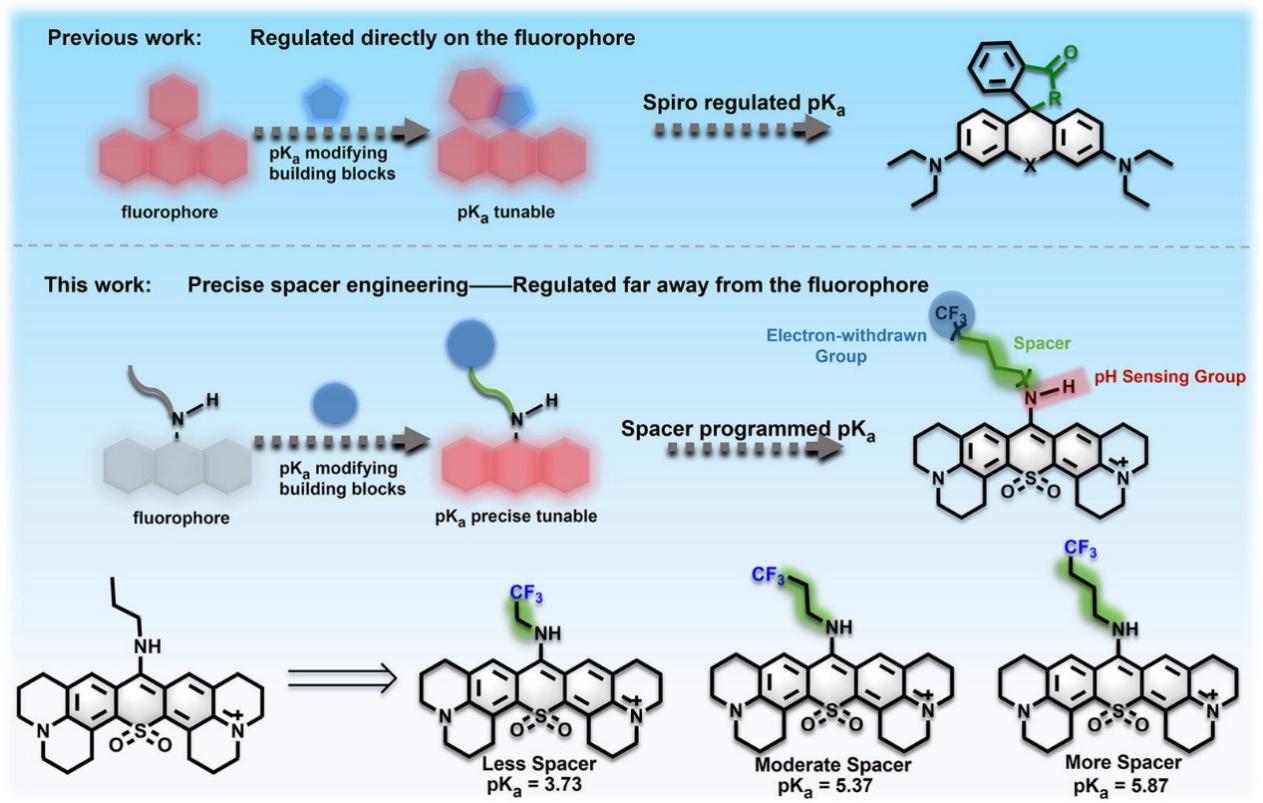
图2 已报道的pKa调控策略以及本研究提出的基于间隔基的pKa调控新策略
通过“间隔基分子工程”的精准pKa调控,作者确定了具有3个间隔基(亚甲基)的探针J-S-BCF3(pKa 5.87)表现出最优的泛癌种成像能力。该探针经静脉注射后,能在胶质瘤、肝癌和乳腺癌等多种原位肿瘤模型中实现快速荧光激活,T/N值分别为2.20、1.97和3.29,同时具有可靠的肿瘤边界描绘能力(图2)。更值得关注的是,该探针成功实现了微淋巴结转移和肺转移灶的高对比度成像,解决了转移瘤诊断灵敏度不足的难题,为转移瘤的早期检测提供了新工具。
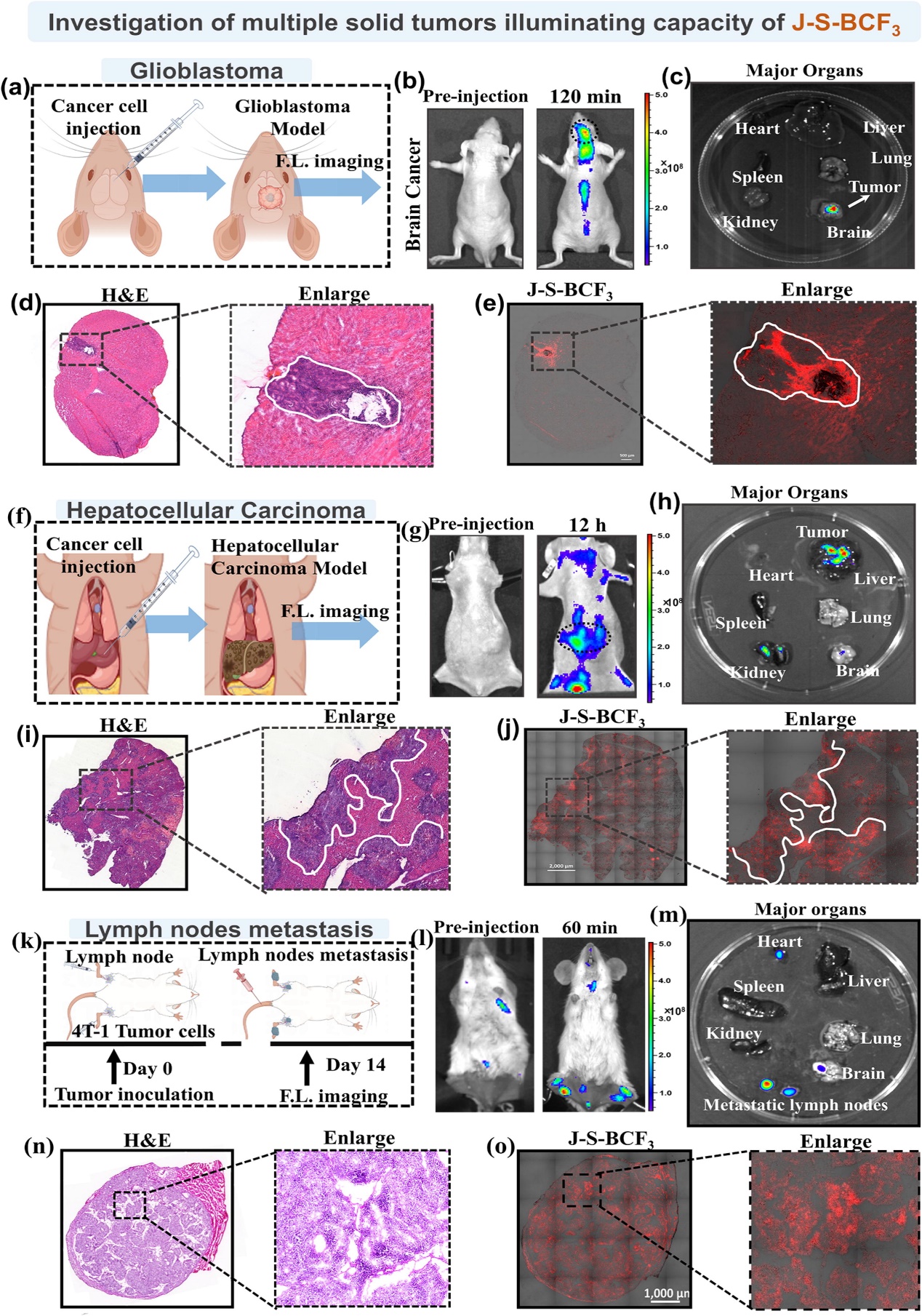
图3 探针J-S-BCF3对原位肿瘤(胶质瘤、肝癌和乳腺癌)的体内荧光成像评价
此外,借助该探针的荧光高通量筛选功能,团队从天然生物碱中成功鉴定出利血平作为潜在V-ATP酶抑制剂,并实时监测到利血平处理后肿瘤微环境的碱化重塑过程(图3)。结合RNA测序和蛋白质印迹分析的机制研究表明,利血平可通过抑制V-ATP酶活性减少质子外排,进而上调肿瘤微环境pH值。
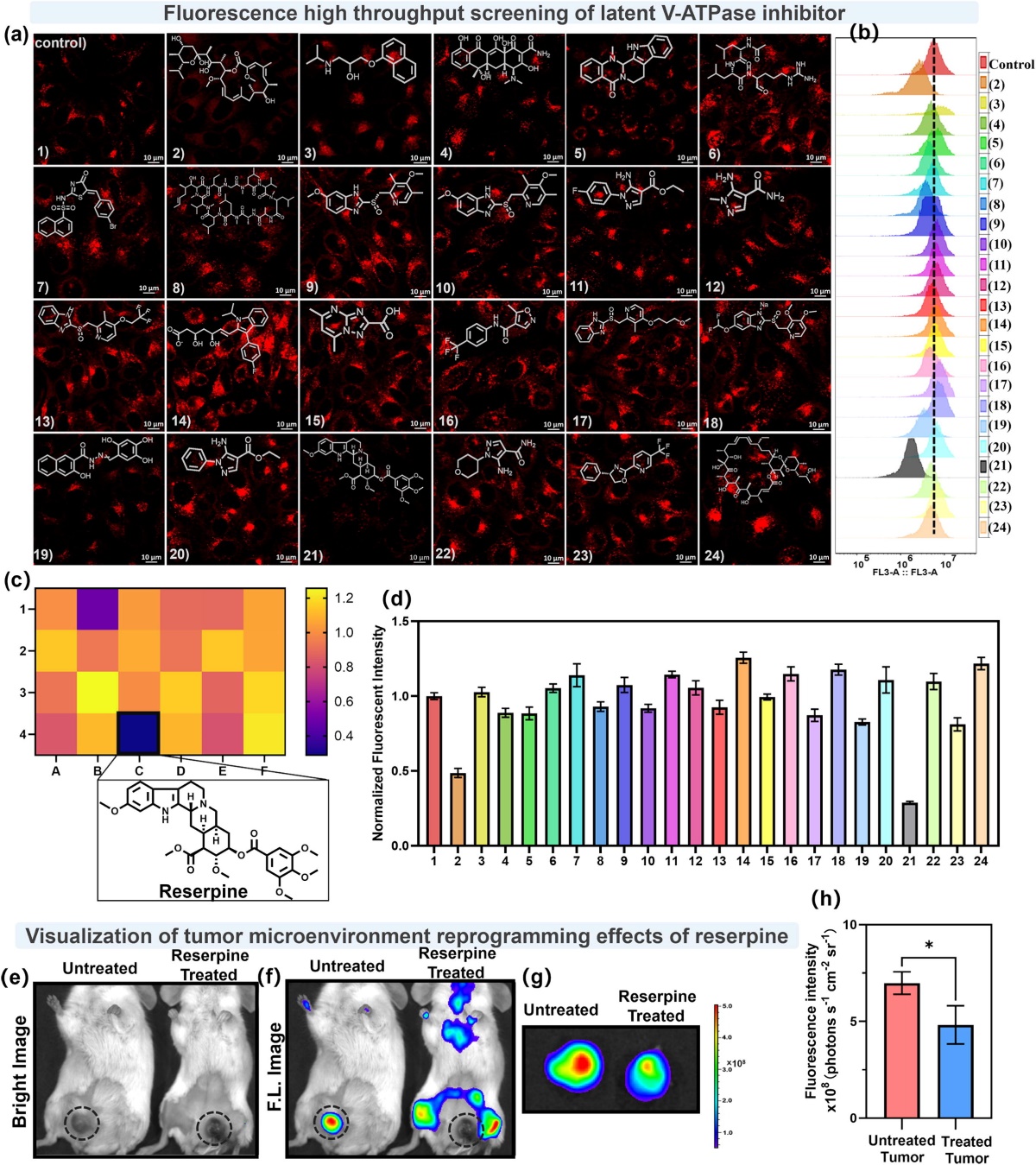
图4 高通量筛选潜在的V-ATP酶抑制剂以及监测利血平诱导的肿瘤微环境重编程
总体而言,这项研究建立了采用间隔基远程调控荧光团特性的分子工程新策略,不仅拓宽了可调谐、高性能荧光探针的构建思路,为下一代荧光探针的开发提供参考,其筛选的探针J-S-BCF₃ 也在泛癌检测、微转移灶成像及肿瘤微环境重塑评估中展现出极大的应用潜力。
责编:曾益
编审:范佳