近日,西华大学余孝其教授团队在国际顶级期刊《JACS Au》(IF=8.7)发表题为“Liberating Exciton Transfer as a Pioneering Strategy to Construct Type I Photosensitizers for Hypoxia Deep-Seated Metastases Suppression”的研究论文,利用新策略构建I型光敏剂,为乳腺癌肺转移治疗开辟新路径。

论文截图(一)
光动力治疗(PDT)作为精准医疗领域的重要技术,凭借时空精准、无创性、不易产生耐药性等优势,已广泛应用于肿瘤治疗、抗菌治疗等领域。其核心是通过光敏剂(PSs)将光能转化为细胞毒性活性氧(ROS),从而杀伤病变细胞。然而,传统II型光敏剂严重依赖肿瘤微环境中的氧气生成单线态氧,而实体肿瘤普遍存在的缺氧问题,导致治疗效果大打折扣,制约了光动力治疗的发展。相较于II型光敏剂,I型光敏剂通过电子转移途径,可利用氧气、水等分子生成超氧阴离子、羟基自由基等不依赖氧气的活性氧,为缺氧肿瘤治疗提供了理想解决方案。但长期以来,缺乏通用的分子设计调控策略,导致I型光敏剂的研发进展缓慢。
针对这一挑战,两个团队提出“激子转移释放”创新策略,成功设计合成系列高性能I型光敏剂:以富电子的硅杂蒽为电子给体,构建具有大扭转角的强给体—受体(D-A)体系,并通过卤素(F、Cl、Br)修饰作为“精准钩子”,打破三重态激子的“笼缚”状态,使其更自由地迁移并与底物高效作用。
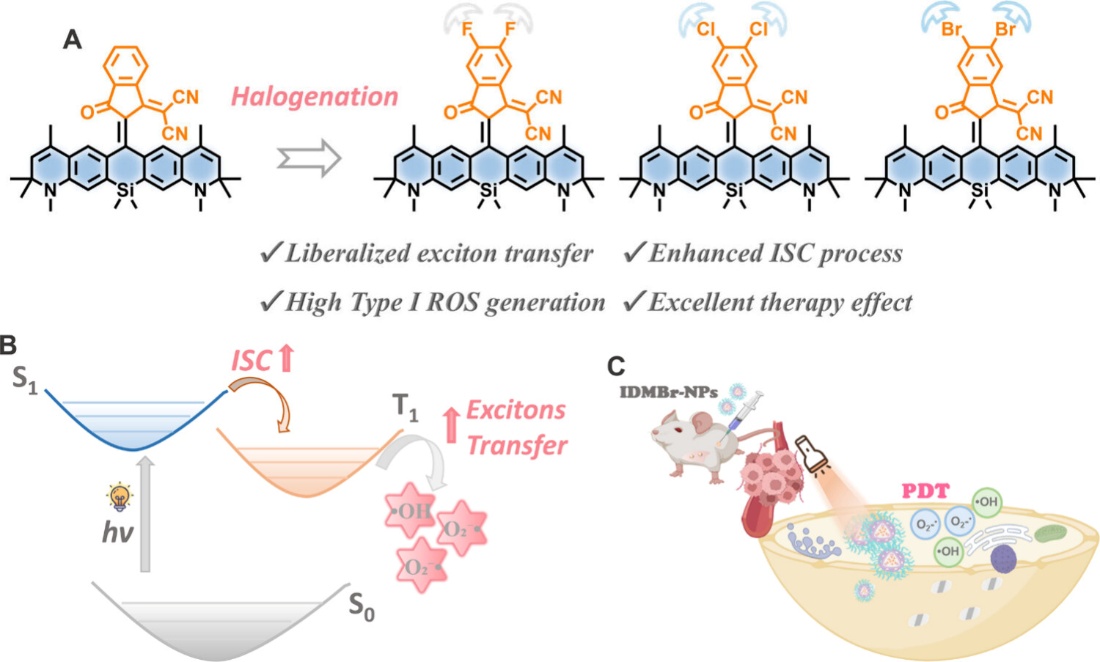
论文截图(二)
无论是正常氧环境还是缺氧条件下,IDMBr-NPs在细胞中均能高效产生活性氧,对三阴性乳腺癌4T1细胞具有强效杀伤,能有效实现其3D细胞球的有效消融,验证了其针对实体肿瘤的治疗潜力。针对三阴性乳腺癌易转移的临床痛点,团队将IDMBr光动力治疗与PD-1抗体免疫治疗相结合,成功实现了肿瘤消融与肺转移抑制的双重效果—联合治疗组小鼠肺部转移结节面积显著减小,肿瘤组织中CD4+和CD8+T细胞浸润明显增强,为晚期转移性肿瘤治疗提供了协同方案。
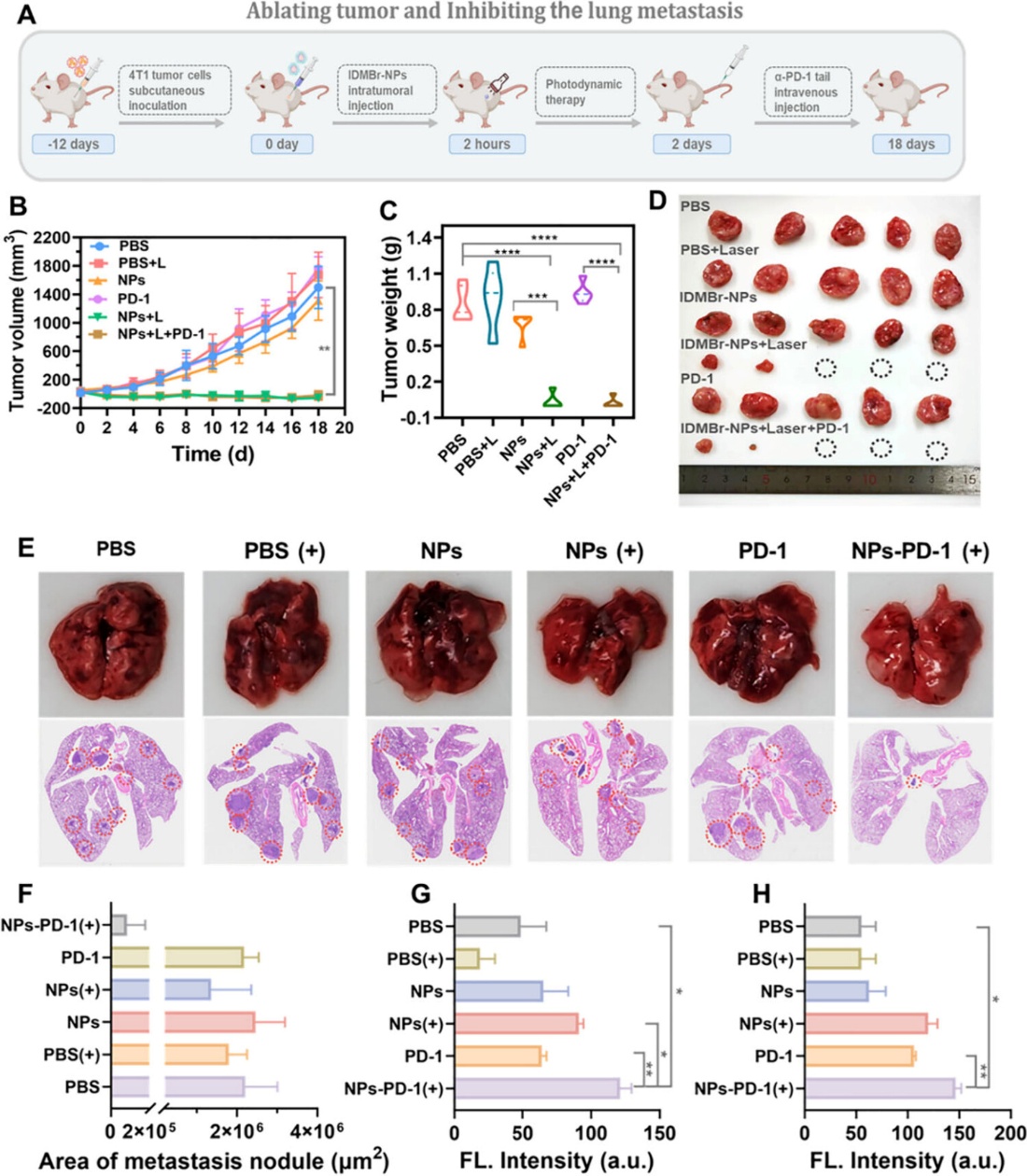
论文截图(三)
该研究为I型光敏剂的理性设计提供了新思路,突破了传统光动力治疗依赖氧气的局限。IDMBr光敏剂在缺氧深层肿瘤治疗中的优异表现,有望推动光动力治疗在晚期肿瘤临床应用中的进一步应用。
责编:曾益
编审:范佳